আইসোটোপ কাকে বলে? সংজ্ঞা, বৈশিষ্ট্য ও উদাহরণ
ভূমিকা
রসায়ন বিজ্ঞানের একটি গুরুত্বপূর্ণ বিষয় হলো পরমাণু ও মৌল। প্রতিটি মৌল ছোট ছোট কণার মাধ্যমে গঠিত, যেগুলোকে বলা হয় পরমাণু। একটি পরমাণুর ভেতরে থাকে প্রোটন, নিউট্রন এবং ইলেকট্রন। সাধারণভাবে একটি মৌলের সব পরমাণু একই ধরনের হয়।
তবে কখনো কখনো একই মৌলের কিছু পরমাণুর গঠন সামান্য ভিন্ন হতে পারে। অর্থাৎ প্রোটনের সংখ্যা একই থাকলেও নিউট্রনের সংখ্যা ভিন্ন হতে পারে। এই ধরনের পরমাণুগুলোকে বলা হয় আইসোটোপ।
মাধ্যমিক ও উচ্চমাধ্যমিক স্তরের শিক্ষার্থীদের জন্য আইসোটোপ কাকে বলে এবং এর উদাহরণ জানা খুবই গুরুত্বপূর্ণ। এই আর্টিকেলে আমরা সহজ ভাষায় আইসোটোপের সংজ্ঞা, বৈশিষ্ট্য এবং উদাহরণ আলোচনা করবো।
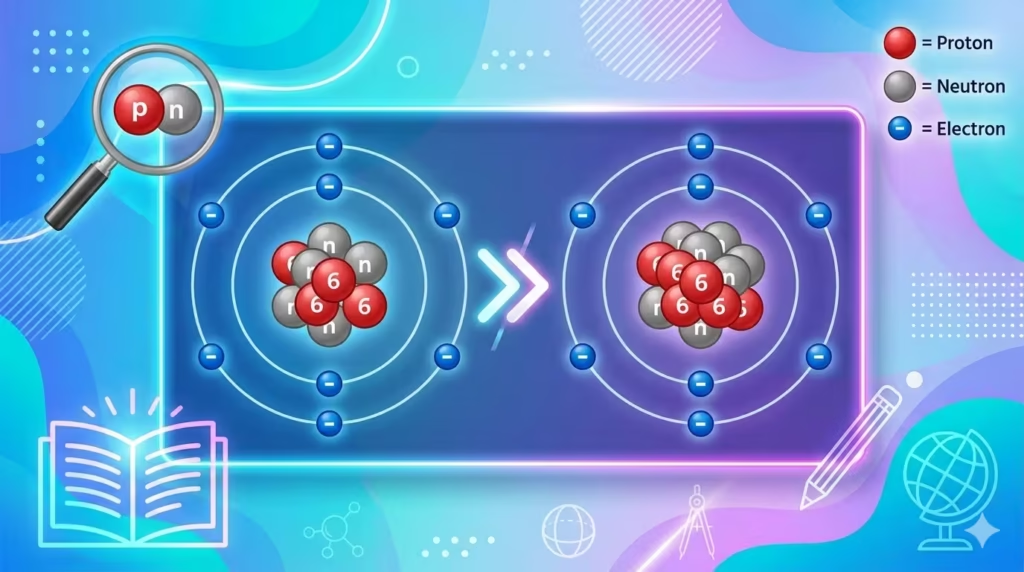
আইসোটোপ কাকে বলে (সংজ্ঞা)
একই মৌলের সেইসব পরমাণুকে আইসোটোপ বলা হয় যাদের পারমাণবিক সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন।
অর্থাৎ, একটি মৌলের পরমাণুগুলোর প্রোটনের সংখ্যা একই থাকে, কিন্তু নিউট্রনের সংখ্যা ভিন্ন হতে পারে। এর ফলে তাদের ভরসংখ্যা আলাদা হয়।
সহজভাবে বলতে গেলে, একই মৌলের ভিন্ন ভরবিশিষ্ট পরমাণুকে আইসোটোপ বলা হয়।
উদাহরণ হিসেবে ধরা যায় হাইড্রোজেন মৌলকে। হাইড্রোজেনের তিনটি আইসোটোপ রয়েছে এবং তাদের পারমাণবিক সংখ্যা একই হলেও ভরসংখ্যা আলাদা।
আইসোটোপের বৈশিষ্ট্য
আইসোটোপের কয়েকটি গুরুত্বপূর্ণ বৈশিষ্ট্য রয়েছে। এগুলো জানলে আইসোটোপ সম্পর্কে ধারণা আরও পরিষ্কার হয়।
১. পারমাণবিক সংখ্যা একই
আইসোটোপ একই মৌলের হওয়ায় তাদের পারমাণবিক সংখ্যা সমান থাকে। অর্থাৎ প্রোটনের সংখ্যা একই।
২. ভরসংখ্যা ভিন্ন
আইসোটোপের ভরসংখ্যা এক নয়। কারণ তাদের নিউট্রনের সংখ্যা ভিন্ন হয়।
৩. রাসায়নিক ধর্ম প্রায় একই
যেহেতু প্রোটনের সংখ্যা একই থাকে, তাই আইসোটোপগুলোর রাসায়নিক ধর্ম সাধারণত একই রকম হয়।
৪. ভৌত ধর্ম ভিন্ন হতে পারে
ভরসংখ্যা ভিন্ন হওয়ার কারণে আইসোটোপগুলোর কিছু ভৌত ধর্ম আলাদা হতে পারে।
৫. একই মৌলের বিভিন্ন রূপ
আইসোটোপ মূলত একটি মৌলের বিভিন্ন রূপ বা প্রকার।
আইসোটোপের উদাহরণ
নিচে কয়েকটি গুরুত্বপূর্ণ আইসোটোপের উদাহরণ দেওয়া হলো।
১. হাইড্রোজেনের আইসোটোপ
হাইড্রোজেনের তিনটি প্রধান আইসোটোপ রয়েছে—
- প্রোটিয়াম (¹H)
- ডিউটেরিয়াম (²H)
- ট্রিটিয়াম (³H)
এই তিনটির পারমাণবিক সংখ্যা একই কিন্তু ভরসংখ্যা ভিন্ন।
২. কার্বনের আইসোটোপ
কার্বনের কয়েকটি আইসোটোপ হলো—
- কার্বন-১২ (¹²C)
- কার্বন-১৩ (¹³C)
- কার্বন-১৪ (¹⁴C)
এগুলোর পারমাণবিক সংখ্যা একই হলেও নিউট্রনের সংখ্যা ভিন্ন হওয়ায় ভরসংখ্যা আলাদা।
৩. ইউরেনিয়ামের আইসোটোপ
ইউরেনিয়ামের দুটি গুরুত্বপূর্ণ আইসোটোপ হলো—
- ইউরেনিয়াম-২৩৫ (²³⁵U)
- ইউরেনিয়াম-২৩৮ (²³⁸U)
এই আইসোটোপগুলো পারমাণবিক শক্তি উৎপাদনে ব্যবহৃত হয়।
আইসোটোপের উপসংহার
আইসোটোপ রসায়নের একটি গুরুত্বপূর্ণ ধারণা। একই মৌলের সেইসব পরমাণু যাদের পারমাণবিক সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন, তাদের আইসোটোপ বলা হয়।
আইসোটোপগুলোর রাসায়নিক ধর্ম প্রায় একই হলেও নিউট্রনের সংখ্যা ভিন্ন হওয়ার কারণে তাদের ভরসংখ্যা এবং কিছু ভৌত ধর্ম আলাদা হয়। বিজ্ঞান ও প্রযুক্তির বিভিন্ন ক্ষেত্রে আইসোটোপের ব্যবহার রয়েছে, যেমন চিকিৎসা, গবেষণা এবং শক্তি উৎপাদনে।
তাই ছাত্রছাত্রীদের জন্য আইসোটোপ কাকে বলে এবং এর উদাহরণ সম্পর্কে পরিষ্কার ধারণা থাকা খুবই গুরুত্বপূর্ণ।




